Michael Faraday
Para analisar mais detalhadamente o fenômeno da indução magnética, Faraday lançou mão de um conceito que ele mesmo havia criado: o de linhas de força, que hoje conhecemos por linhas de campo.
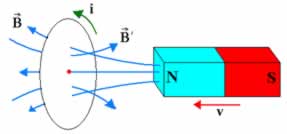
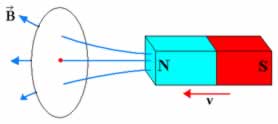
Embora o número de linhas de campo seja obviamente infinito, ele convencionou que, para representar um campo magnético, a densidade das linhas seria proporcional à intensidade do campo. O cálculo dessa densidade das linhas baseia-se na verificação de quantas linhas existem para cada metro quadrado de determinada superfície plana perpendicular a essas linhas, como mostra a figura abaixo.

Desta forma, podemos dizer que o número de linhas que atravessa uma superfície plana, de área A, colocada perpendicularmente a um campo magnético, é proporcional ao produto do campo magnético pela área da superfície, (B . A). Esse produto recebeu o nome de fluxo de B (ou fluxo magnético) através da superfície, sendo representado por ϕ. Assim, temos:

Onde:
ϕ – fluxo magnético
B – campo magnético
A – área da superfície plana
De acordo com a figura abaixo temos uma espira de área A imersa em um campo magnético uniforme. O ângulo formado entre o campo B e o vetor n normal ao plano da espira é θ. Assim, para calcular o fluxo magnético B através da espira temos que levar em consideração o ângulo. Portanto, temos que:

No SI (Sistema Internacional de Unidades) a unidade de fluxo denomina-se weber (Wb).
Por Domiciano Corrêa Marques da Silva
Graduado em Física
Embora o número de linhas de campo seja obviamente infinito, ele convencionou que, para representar um campo magnético, a densidade das linhas seria proporcional à intensidade do campo. O cálculo dessa densidade das linhas baseia-se na verificação de quantas linhas existem para cada metro quadrado de determinada superfície plana perpendicular a essas linhas, como mostra a figura abaixo.

Linhas de campo magnético atravessando uma superfície plana
Desta forma, podemos dizer que o número de linhas que atravessa uma superfície plana, de área A, colocada perpendicularmente a um campo magnético, é proporcional ao produto do campo magnético pela área da superfície, (B . A). Esse produto recebeu o nome de fluxo de B (ou fluxo magnético) através da superfície, sendo representado por ϕ. Assim, temos:
Onde:
ϕ – fluxo magnético
B – campo magnético
A – área da superfície plana
De acordo com a figura abaixo temos uma espira de área A imersa em um campo magnético uniforme. O ângulo formado entre o campo B e o vetor n normal ao plano da espira é θ. Assim, para calcular o fluxo magnético B através da espira temos que levar em consideração o ângulo. Portanto, temos que:
Por Domiciano Corrêa Marques da Silva
Graduado em Física

 de modo que o fluxo de (
de modo que o fluxo de (